On définit pour le point d’acupuncture une sélectivité (différence d’action entre deux points d’acupuncture) et une spécificité (différence d’action entre un point et un non-point). Une équipe de neurobiologistes de la Harvard Medical School a réalisé une avancée majeure dans la compréhension du mécanisme de ce qui constitue la base même de l’acupuncture (Liu 2021 [1]).
L’étude a été publiée en octobre 2021 dans Nature, une des revues scientifiques les plus prestigieuses. L’auteur principal est Ma Qiufa, professeur de neurobiologie au Blavnik Institute de la Harvard Medical school (institution n°1 dans les classements mondiaux) et au Dana-Farber Cancer Institute. Travaillant sur les mécanismes fondamentaux de la douleur, Ma Qiufa s’est tout naturellement intéressé à l’acupuncture, d’autant que d’origine chinoise il a fait la première partie de ses études en Chine avant d’émigrer en 1992 aux USA.
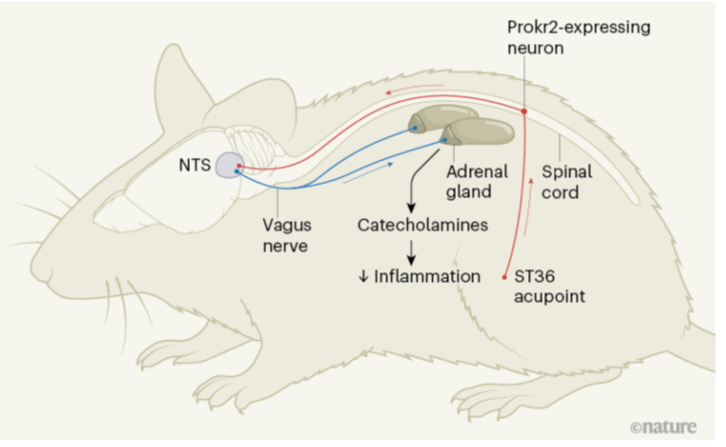
Action de l’acupuncture via le système nerveux autonome : deux axes distincts dépendants du point, de l’intensité et du moment de stimulation (2020).
L’attention de l’équipe a été attirée par un article publié en 2014 dans Nature Medicine. Il était étudié, chez la souris, l'action de l'acupuncture dans un modèle de péritonite induite par injection d’endotoxine bactérienne + ligature et ponction du cæcum (Torres-Rosas 2014 [2]). L'acupuncture permettait une augmentation du taux de survie des animaux. Il était montré que la stimulation du 36E permettait le contrôle de l’inflammation systémique via un axe vago-surrénalien avec libération de dopamine au niveau de la médullosurrénale, la dopamine inhibant la production de cytokines pro-inflammatoires.
Travaillant sur cette donnée initiale, l'équipe de Harvard a montré dans une première publication (Liu 2020 [3]), que l’action anti-inflammatoire de l’acupuncture pouvait passer en fait par deux voies efférentes distinctes du système nerveux autonome visant à la production de catécholamines (adrénaline, noradrénaline et dopamine) [figure 1] :
- Un axe vago-surrénalien agissant via les cellules chromaffines surrénaliennes.
- Un axe spino-sympathique via les neurones noradrénergiques du système nerveux périphérique.
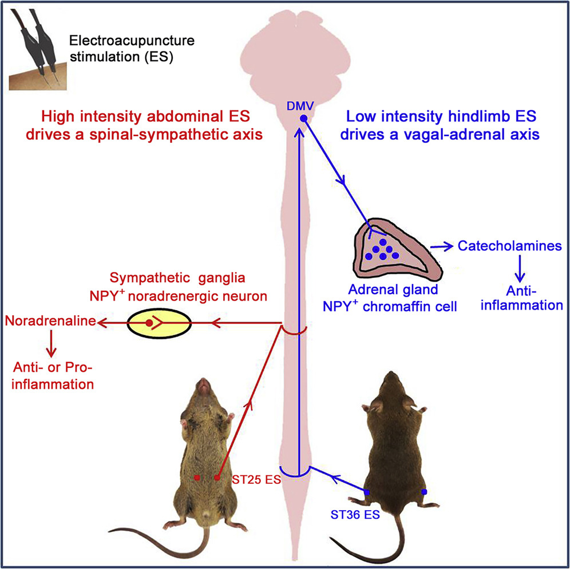
Ils ont travaillé sur un modèle d’inflammation systémique chez la souris induit par les lipopolysaccharides (LPS, endotoxines des bactéries à Gram négatif). Pour la démonstration, ils ont utilisé de nouveaux outils permettant d’étudier sélectivement des sous-types et sous-circuits neuronaux. Ainsi, à l'aide de techniques de génétique intersectionnelle, ils ont réalisé une ablation spécifique d'une part des neurones noradrénergiques NPY+ et d'autre part des cellules chromaffines NPY+ surrénaliennes. Cela leur a permis de comparer la réponse à l'inflammation chez les souris avec ou sans ces cellules cibles pour déterminer si et comment elles étaient impliquées dans la modulation de l'inflammation. De manière concluante, ces cellules nerveuses apparaissent comme des éléments clés de l'action anti-inflammatoire de l’acupuncture.
De plus, l'équipe a montré que la réponse de l’acupuncture dépendait de trois facteurs : le point, l’intensité et le moment de stimulation.
- Le point. Une stimulation à basse intensité (0.5 mA) induit une réponse vago-surrénalienne au 36E (zusanli) mais pas au 25E (tianshu).
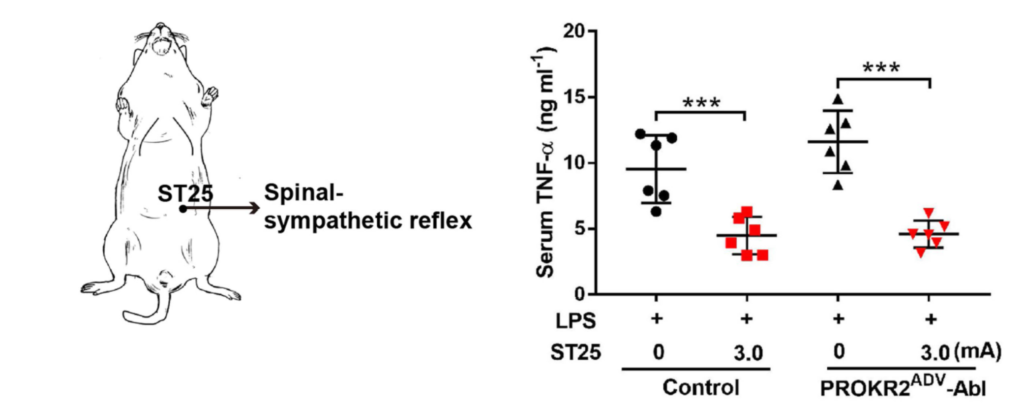
- l'intensité. Inversement une stimulation à haute intensité (3.0 mA) non à basse intensité (0.5 mA) du 36E ou du 25E entraine une réponse anti-inflammatoire spino-sympathique, et non vago-surrénalienne.
- le moment du traitement. L’acupuncture à haute intensité du 25E produit des effets anti- ou pro-inflammatoires selon le moment où le traitement est effectué. Si le traitement est appliqué préventivement une réponse anti-inflammatoire avec diminution de la tempête de cytokines est observée et augmente la survie des animaux de 20 à 80%. Inversement si l’acupuncture est appliquée après, l’inflammation est aggravée et la survie diminuée. Ceci suppose l’activation de récepteurs différents.
L'activation des effets anti-inflammatoires de l'acupuncture est donc spécifique à certains points d'acupuncture (somatotopie), à des niveaux spécifiques d'intensité d'électroacupuncture et fonction de l’état pathologique. Les paramètres optimaux de la stimulation acupuncturale devront donc être soigneusement définis autant pour des raisons d’efficacité que de sécurité.
Sur la base de ces données, l'équipe a alors émis l'hypothèse que ces différences de réponse pourraient être liées à la présence de neurones sensoriels spécifiques dans la région du 36E. C’est l’objet de l’étude de 2021.
Les neurones exprimant Prokr2, base cellulaire de l’action anti-inflammatoire du 36E à basse intensité (2021).
Le résultat majeur du récent article de Nature de 2021 est la mise en évidence d’un sous-type de neurones comme base neuroanatomique de l’action antiinflammatoire de l’acupuncture via la voie vago-surrénalienne.
Caractérisation des neurones Prokr2
Dans un premier temps les auteurs ont caractérisé chez la souris une population de neurones sensoriels génétiquement marqués par l’expression du récepteur Prokr2 (Prokr2cre ou Prokr2adv).
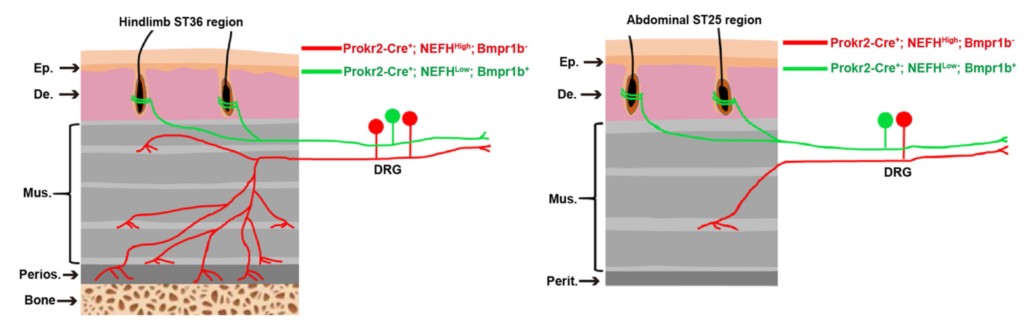
- Ces neurones génétiquement marqués sont une population mixte avec deux sous-types, certains innervant les follicules pileux ( Nefhlow) et d’autres innervant les tissus profonds, tels que les tissus fasciaux (Nefhhigh) (figure 2).
- Si les Nefhhigh innervent les tissus fasciaux des membres postérieurs (par exemple le périoste au niveau du 36E), ils n’innervent pas les fascias abdominaux (par exemple le péritoine au niveau du 25E). La distinction entre 25E et 36E est donc dans une sous-population de neurones Prokr2.
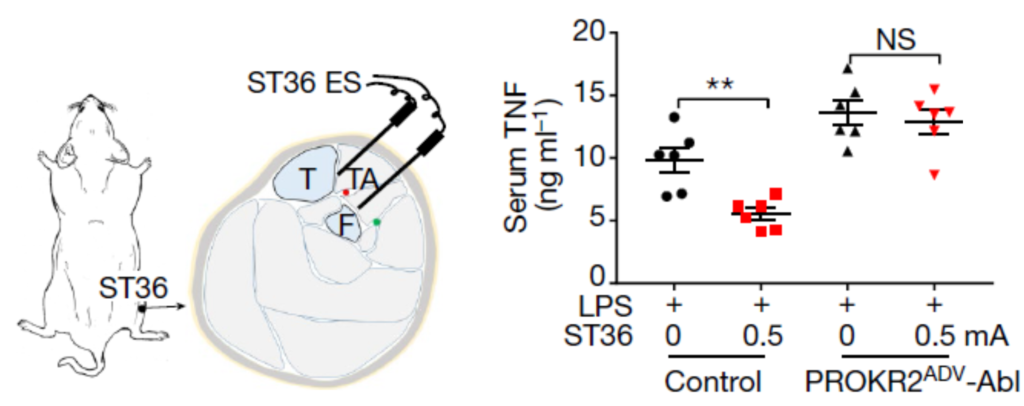
Implication des neurones de la lignée Prokr2 dans l’action du 36E,
Comme dans l’étude de 2020, les auteurs utilisent un modèle d’inflammation systémique induite par LPS. La stimulation à faible intensité (0.5 mA) du 36E induit :
- une expression de la protéine c-Fos au niveau des neurones du noyau dorsal du vague, témoin de l’activation neuronale à ce niveau ;
- la libération de catécholamines et de dopamine ;
- la réduction des cytokines pro-inflammatoires TNF et IL-6 (fig. 3) ;
- une élévation de la survie des animaux (fig. 7).
Pour démontrer l’implication des neurones Prokr2 , les chercheurs ont mené une série d’élégantes expériences génétiques de perte de fonction (ablation sélective) et de gain de fonction (stimulation optogénétique).
Ablation sélective
L'ablation sélective des neurones sensoriels marqués par Prokr2cre inhibe toutes les réponses observées : expression de c-Fos, libération de catécholamine, baisse des TNF et IL-6 et survie des animaux (fig. 3 et 7).
Par contre l’action anti-inflammatoire du 36E et du 25E à haute intensité (3.0 mA) n’est pas affectée par l’ablation des neurones Prokr2 (fig. 4).
En conclusion les neurones Prokr2 sont requis pour une action de l'électroacupuncture basse intensité à visée anti-inflammatoire par l’axe vago-surrénalien.
La stimulation optogénétique
L'optogénétique s'appuie sur l'insertion dans la membrane d'une cellule nerveuse de molécules sensibles à la lumière qui, sous l'effet d'une stimulation lumineuse, vont modifier l'état de polarisation de la membrane. Cela revient à pouvoir activer optiquement la cellule modifiée et les cellules de son réseau (fig. 5).
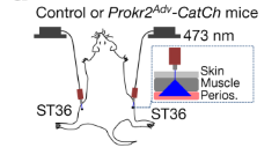
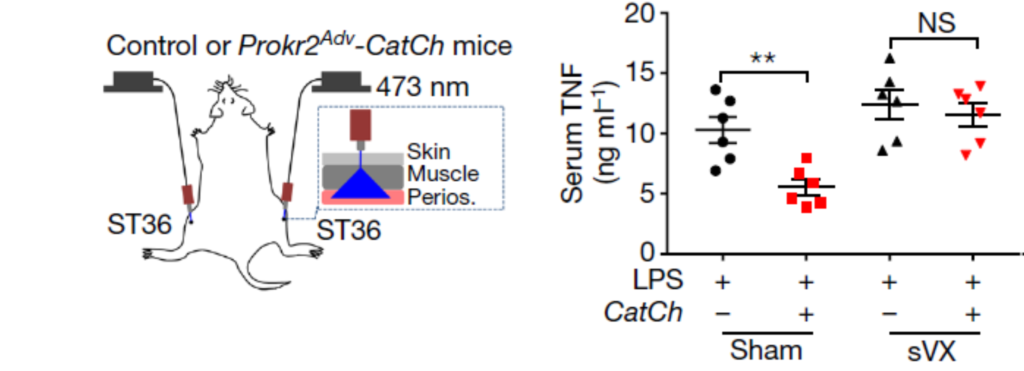
La stimulation optogénétique (les auteurs vont jusqu'à parler d’opto-acupuncture) des fibres nerveuses Prokr2 au niveau du 36E est suffisante pour entraîner l'axe anti-inflammatoire vago-surrénalien avec les mêmes réponses que l’acupuncture : coloration c-Fos, catécholamine, dopamine, TNF (fig. 6) et taux de survie (fig. 7). Ces effets sont supprimés après vagotomie (fig. 6). Mais la stimulation optogénétique est par contre incapable d'activer la voie spino-sympathique.
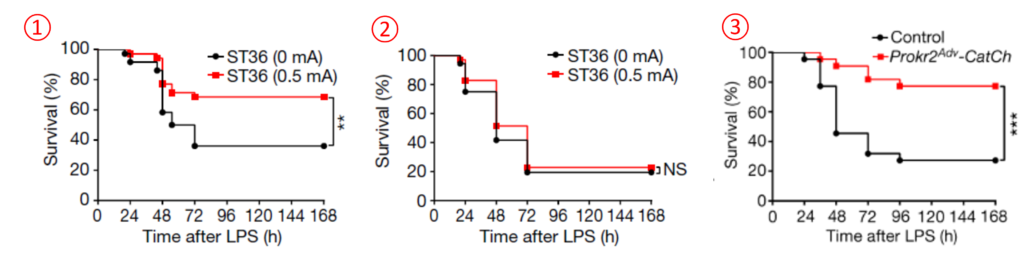
En conclusion, la stimulation optogénétique avec stimulation spécifique des neurones Prokr2 reproduit l'action de l'électroacupuncture à basse intensité.
Nécessité d’une puncture profonde
La différence identifiée entre le 36E et le 25E est la présence au niveau profond de neurones Prokr2 Nefhhigh . Pour vérifier l'importance de la profondeur de puncture dans la mise en jeu de la réponse anti-inflammatoire à l'acupuncture à haute intensité, d'autres expériences ont été conduites :
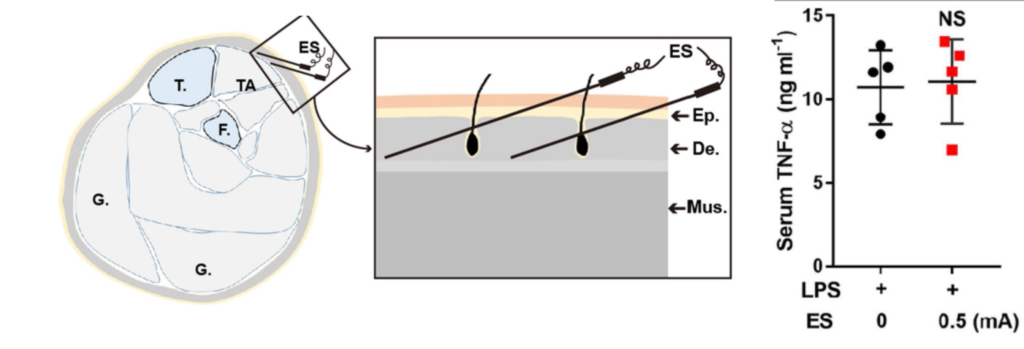
- L'effet attendu de la stimulation du 36E se produit à une puncture profonde (0.3 mm chez le rat) mais non à une puncture superficielle cutanée (fig. 8).
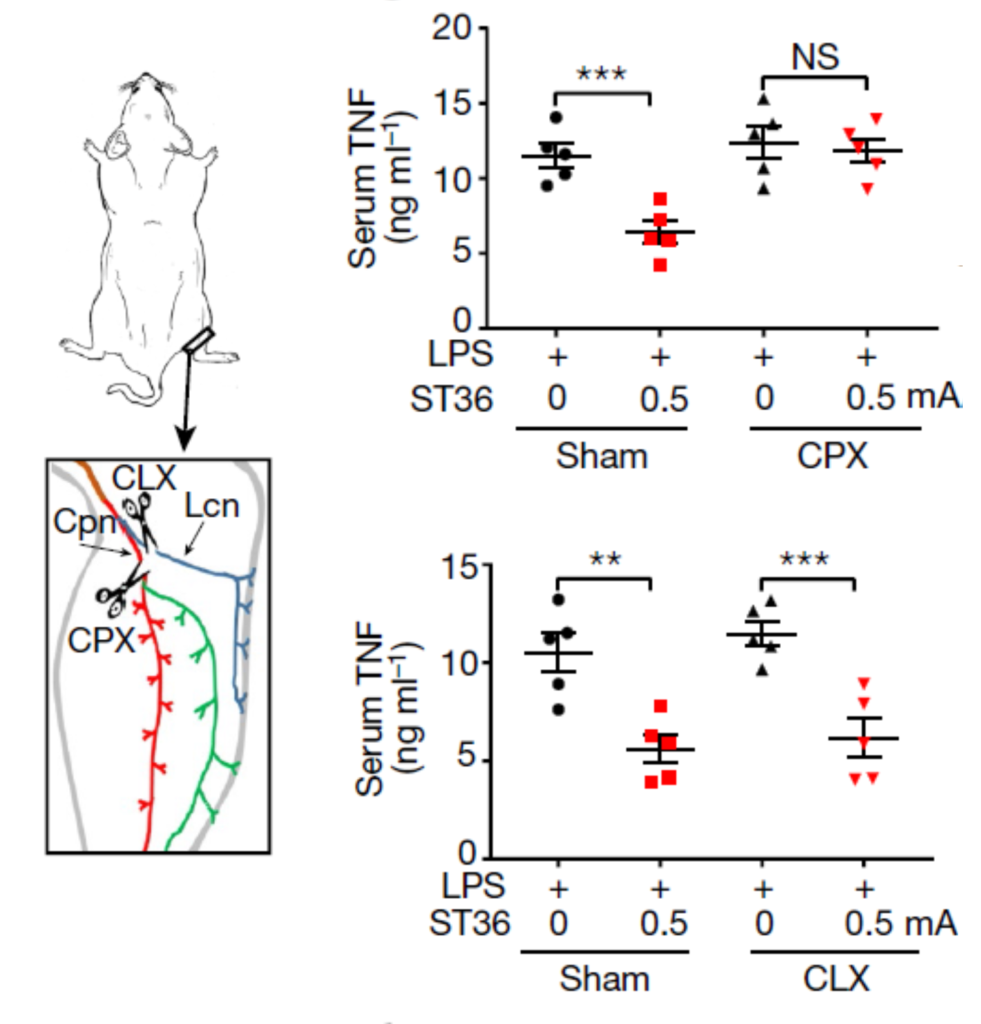
- La section du fibulaire commun qui innerve le niveau profond, mais non celle du cutané latéral qui innerve le niveau superficiel supprime l'effet attendu de la stimulation du 36E (fig. 9).
- Absence d'effet à la stimulation du nerf sural qui est superficiel au niveau de chengjin (56V).
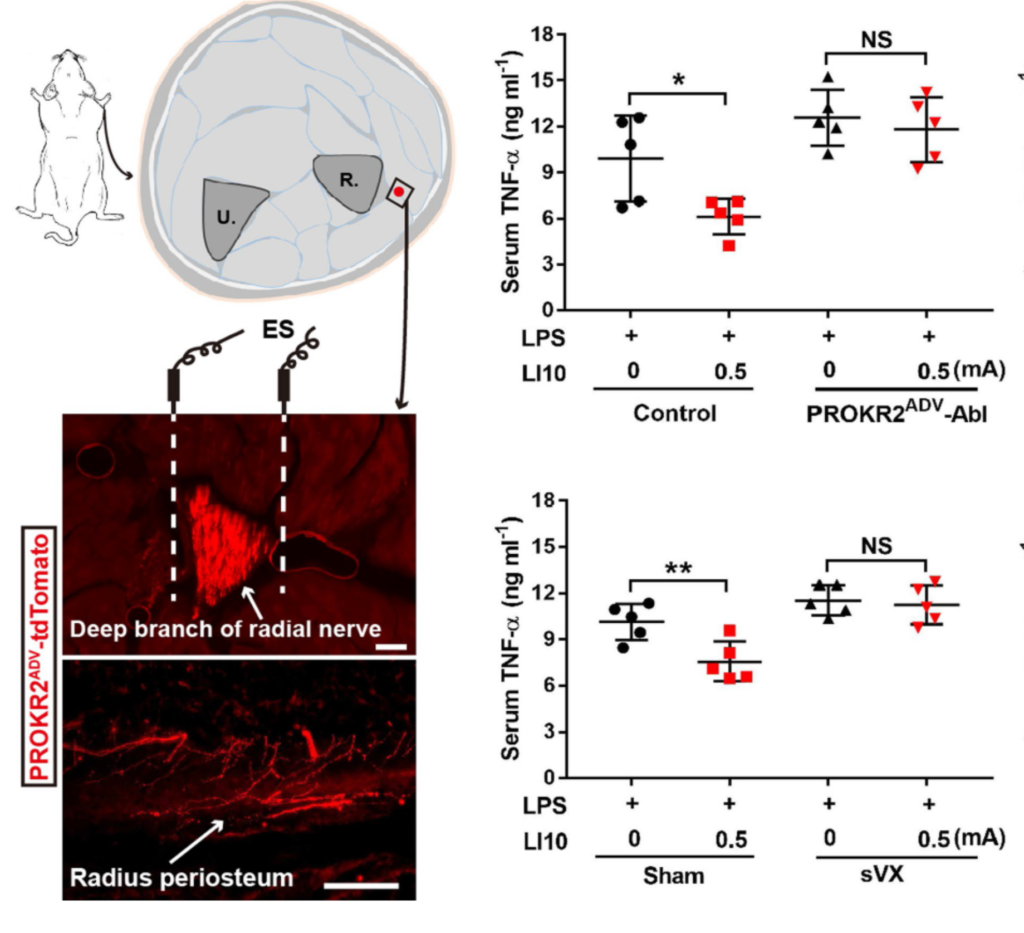
Shousanli (10GI) a la même population de neurones et la même action que zusanli (36E)
L'effet de la stimulation à basse intensité du 36E s'observe également au niveau du 10GI (shousanli) où on relève la présence de neurones Prokr2 (fig. 10).
Conclusions
Les auteurs ont donc montré que la spécificité d'action du 36E sur l'inflammation systémique via la voie vago-surrénalienne était liée à la présence d'un sous-ensemble particulier de neurones. L'activation de ces neurones est à la fois nécessaire et suffisante pour cet effet.
Cela laisse supposer que la sélectivité et la spécificité des points d'acupuncture pourraient être liées à diverses sous-populations neuronales dont la distribution spatiale somatique et la spécialisation s'est effectuée au cours de l'embryogénèse.
Mais ces travaux apportent également d'autres types d'informations essentielles pour la recherche en acupuncture et ses applications cliniques :
- L'acupuncture peut agir sur une pathologie donnée par des mécanismes distincts mis en action par des points différents et des modalités de stimulation différentes.
- Parmi ces modalités de stimulation, deux paramètres sont identifiés dans les études rapportées : la profondeur de puncture et l'intensité de stimulation. Il s'agit là de paramètres classiques dans la pratique de l'acupuncture, base par exemple des techniques de tonification/dispersion.
- L'action de l'acupuncture dépend du stade d'une pathologie et de l'état de l'organisme.
Ces considérations sont centrales. Elles expliquent la variabilité et l'hétérogénéité des effets de l'acupuncture observés dans les études cliniques. Elles ouvrent des perspectives dans une compréhension plus fine des mécanismes de l'acupuncture et dans l'élaboration de protocoles d'acupuncture optimaux.
Drs Johan Nguyen et Olivier Goret
Références
- Liu S, Wang Z, Su Y, Qi L, Yang W, Fu M, Jing X, Wang Y, Ma Q. A neuroanatomical basis for electroacupuncture to drive the vagal-adrenal axis. Nature. 2021 Oct;598(7882):641-645. [219458]. |doi|
- Torres-Rosas R, Yehia G, Peña G, Mishra P, del Rocio Thompson-Bonilla M, Moreno-Eutimio MA, Arriaga-Pizano LA, Isibasi A, Ulloa L. Dopamine mediates vagal modulation of the immune system by electroacupuncture. Nat Med. 2014;20(3):291-5. [170886]. |doi| 🔓
- Liu S, Wang ZF, Su YS, Ray RS, Jing XH, Wang YQ, Ma Q. Somatotopic Organization and Intensity Dependence in Driving Distinct NPY-Expressing Sympathetic Pathways by Electroacupuncture. Neuron. 2020;108(3):436-450. [215524]. |doi| 🔓
- Kupari J, Ernfors P. Pricking into Autonomic Reflex Pathways by Electrical Acupuncture. Neuron. 2020;108(3):395-397. [215525]. |doi| 🔓
- Ulloa L. Electroacupuncture activates neurons to switch off inflammation. Nature. 2021 Oct;598(7882):573-574. |doi|
Mots-clés : Acupuncture expérimentale- mécanismes d'action - Points

Pour résumer il faut préférentiellement utiliser la stim basse fréquence du 36E
Plutôt que le 25E en haute fréquence
Lors du dernier congrès au Japon j’avais noté que la basse fréquence 5hz était toujours utilisée –
Merci pour cet article
Amitiés
YM Dantec